


鼎 泰 助 力
鼎泰集團助力RRG001眼内注射液成(chéng)功獲批 鼎泰集團作爲鼎新基因的深度合作夥伴,憑借在眼科藥物評價領域的一體化服務能(néng)力,爲RRG001眼内注射液提供了支持IND申報的全套非臨床研究,包括藥效學(xué)、藥代動力學(xué)、安全性評價。此外,藥政策略團隊緊密跟蹤同類藥物臨床研究進(jìn)展,爲客戶輸出了有競争力的開(kāi)發(fā)策略,并制定了高效的注冊申報路線,高效率、高質量完成(chéng)pre-IND溝通交流和IND申請。基于在研究過(guò)程中建立的友好(hǎo)、互信的合作關系,鼎泰集團眼科團隊將(jiāng)繼續承擔後(hòu)續的臨床試驗相關服務,將(jiāng)爲RRG001快速完成(chéng)早期臨床概念驗證并推進(jìn)至關鍵性臨床試驗提供專業的臨床服務。 對(duì)于RRG001眼内注射液獲批IND的喜訊,鼎泰集團表示熱烈祝賀!也對(duì)後(hòu)期的臨床試驗開(kāi)發(fā)充滿期待與信心!鼎泰集團將(jiāng)與鼎新基因攜手努力,爲nAMD患者帶來更有臨床價值的治療方案! ”
關于RRG001眼内注射液 據鼎新基因新聞稿報道(dào),RRG001眼内注射液是鼎新基因擁有自主知識産權的重組腺相關病毒(rAAV)基因治療藥物,通過(guò)視網膜下腔給藥將(jiāng)血管内皮生長(cháng)因子受體(VEGFR)Fc融合蛋白基因導入nAMD患者眼底,讓眼底細胞成(chéng)爲蛋白工廠,不斷表達患者需要的VEGF受體Fc融合蛋白,避免了傳統抗VEGF抗體藥物需要頻繁玻璃體注射給藥的弊端,以期達到“一次給藥、長(cháng)期獲益”的治療效果。RRG001眼内注射液的藥物設計采用了VEGF受體Fc融合蛋白工程化改造和高效基因表達盒,藥物生産采用高産細胞系、全封閉、一次性、無血清大規模懸浮培養工藝,生産和檢驗全程符合《藥品生産質量管理規範》(GMP)要求。
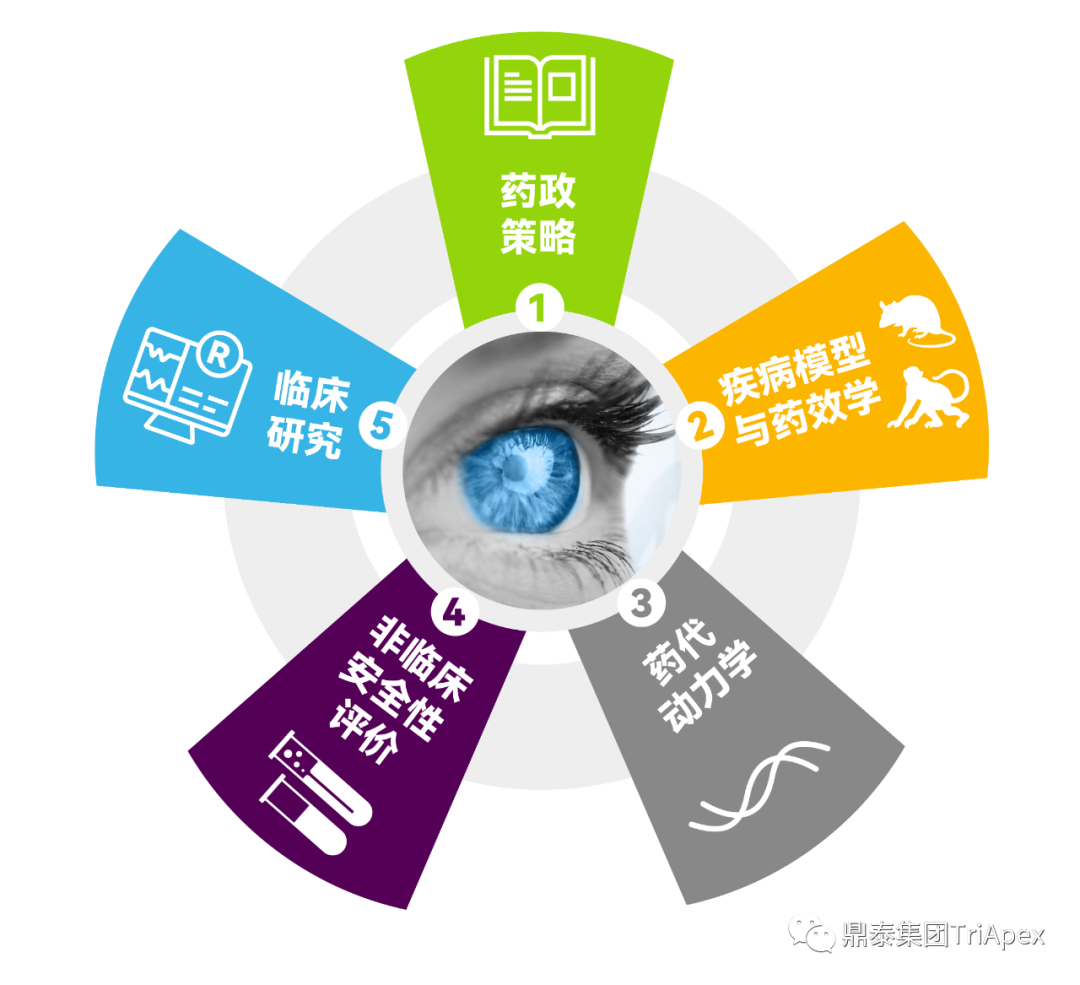
鼎泰集團眼科一體化平台 在眼科藥物或器械評價領域,鼎泰集團擁有從非臨床到臨床的一體化眼科研發(fā)賦能(néng)平台。建立了多種(zhǒng)大/小動物疾病模型,配備有行業頂尖的檢查、檢測分析設備,搭建了深耕眼科數十年的核心科學(xué)家團隊,積累了基因治療類、抗體類、小分子類等多種(zhǒng)眼科藥物的非臨床和臨床評價經(jīng)驗。 眼科領域一體化研發(fā)賦能(néng)平台 多種(zhǒng)屬綜合性眼科臨床檢查能(néng)力 眼科疾病領域一體化研發(fā)賦能(néng)平台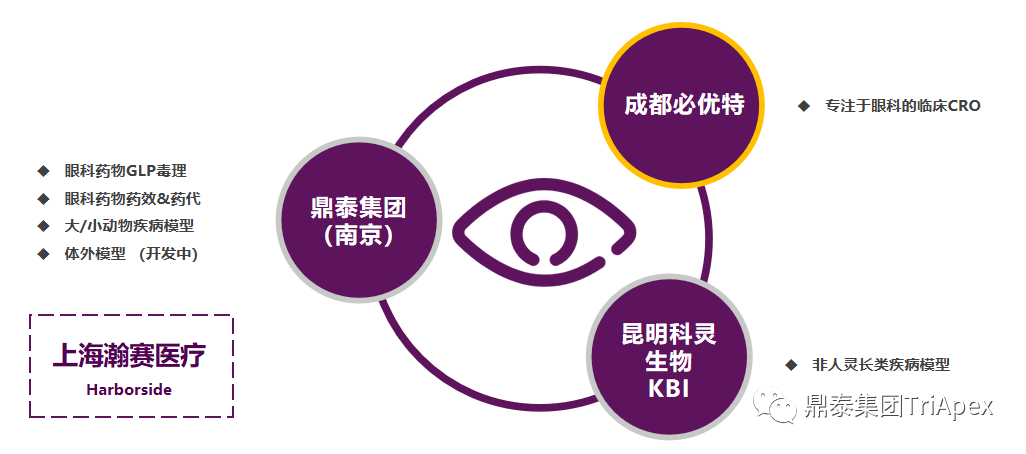

結語 鼎泰集團期待着與更多藥物研發(fā)企業及機構深度合作,共同推動眼科藥物的研究進(jìn)程。我們將(jiāng)繼續秉持“科技創新,造福人類”的理念,助力合作夥伴爲全球眼科疾病患者提供更全面(miàn)、更有效的治療方案!


































